随着我国医疗器械产业的快速发展与监管体系的不断完善,医疗器械产品注册作为市场准入的核心环节,其相关数据不仅是行业发展的风向标,也是监管效能和企业战略决策的重要依据。2018年,在国家药品监督管理局的统一监管下,各省、自治区、直辖市药品监督管理部门受理和审批了大量医疗器械注册申请,形成了一组丰富且极具分析价值的数据集。
一、2018年国内医疗器械注册数据概况
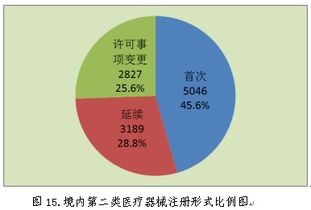
从整体趋势看,2018年国内医疗器械产品注册申请总量继续保持稳健增长,这反映了产业创新活力的持续迸发和市场需求的不断扩大。数据显示,注册申请主要集中在经济发达、医疗资源丰富和产业集聚度高的地区,如广东省、江苏省、上海市、北京市、浙江省等。这些省份不仅在注册数量上领先,在创新型产品,特别是第三类高风险医疗器械的注册申请上也占据显著优势,体现了其强大的研发能力和完整的产业链支持。
与此中西部部分省份的注册数量虽相对较少,但增长速度引人注目,显示出区域产业发展的潜力和国家均衡发展战略的成效。从产品类别分析,体外诊断试剂、无源植入器械、医用成像设备等领域的注册申请较为活跃,与全球医疗技术热点及我国临床需求紧密契合。
二、注册办理数据背后的深层次信息
这些原始的注册办理数据,看似是简单的数字统计,实则蕴含了多维度的信息:
- 区域产业竞争力地图:各省的注册数量、类别构成和审批通过率,直观地绘制出全国医疗器械产业的竞争力分布与集群效应。
- 监管政策落地效果:数据可以反映新修订的《医疗器械监督管理条例》及相关配套文件在各地的执行情况与差异,为优化监管提供参考。
- 技术创新风向标:通过分析获批的创新医疗器械特别审批程序产品分布,可以洞察前沿技术(如人工智能辅助诊断、可穿戴监测、生物3D打印等)的研发重心和产业化进展。
- 企业战略参考系:对于医疗器械生产企业而言,同领域、同地区的注册数据是进行市场进入、竞品分析和研发立项的关键情报。
三、数据处理服务的核心价值与应用场景
面对海量、异构且动态更新的注册数据,专业的数据处理服务变得至关重要。其核心价值在于将原始数据转化为可支持决策的结构化信息与深度洞察。
- 数据清洗与标准化:原始数据可能存在记录不完整、格式不统一、分类口径差异等问题。数据处理服务通过建立统一的数据清洗规则和标准术语库,确保数据的准确性、一致性和可比性。
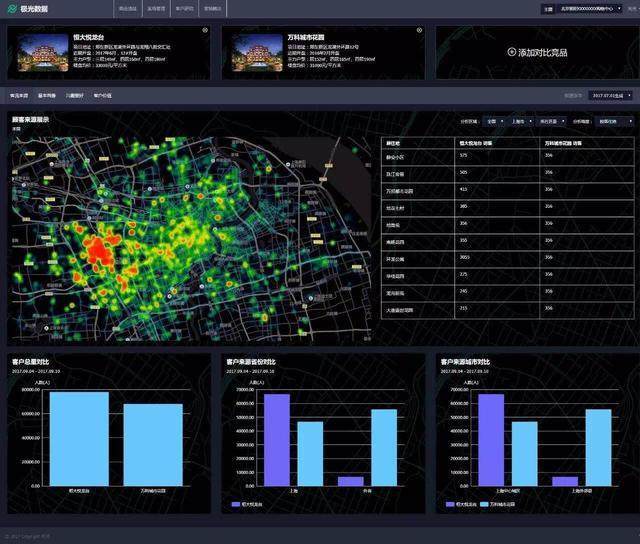
- 多维度分析与可视化:服务提供方利用统计分析、数据挖掘技术,可从时间趋势、地域分布、产品分类、申请人类型、审批周期等多个维度进行交叉分析,并通过图表、仪表盘等可视化形式直观呈现,使复杂数据一目了然。
- 深度报告与定制洞察:超越基础统计,提供深度分析报告,解读数据背后的产业规律、政策影响和市场机遇。例如,针对特定细分领域(如心血管介入、骨科植入物)进行竞争格局分析,或评估某省份的产业投资环境。
- 监测预警与动态跟踪:建立数据监测平台,对特定企业、产品或技术领域的注册动态进行实时跟踪和预警,帮助企业及时把握监管动向和市场竞争态势。
应用场景广泛:
监管机构:用于评估监管效能、优化资源配置、发现区域性风险、制定精准产业扶持政策。
医疗器械企业:用于市场调研、竞品监控、研发方向校准、注册策略优化(如选择优先注册区域)。
投资与咨询机构:用于评估行业赛道热度、企业估值、寻找潜在投资标的。
研究与学术机构:用于开展产业经济、创新扩散、政策评估等相关学术研究。
四、挑战与展望
尽管数据价值巨大,但在利用过程中也面临挑战,如数据公开的颗粒度和时效性有待进一步提高,跨区域、跨平台的数据孤岛现象仍需打破。随着大数据、人工智能技术与监管科学的深度融合,对医疗器械注册数据的处理将更加智能化、实时化和预测化。数据处理服务将不仅局限于事后分析,更可能向前端的注册策略模拟、风险评估预测延伸,为行业健康发展提供更强大的数据引擎。
2018年国内各省医疗器械产品注册办理数据是一座尚待深入挖掘的“富矿”。专业、高效的数据处理服务是打开这座富矿的钥匙,能够为政府监管、产业发展和企业竞争提供不可或缺的数据驱动力,共同助推我国从医疗器械制造大国向制造强国和创新强国迈进。